Melongok Persiapan BPOM Jelang Tenggat Waktu Vaksinasi Covid-19

- BPOM belum juga memberikan lampu hijau vaksin Covid-19 sebelum 13 Januari
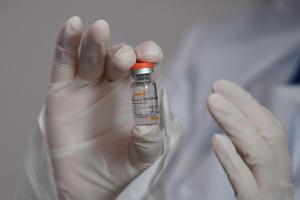
- MUI telah menyatakan vaksin Sinovac halal dan suci
- Biofarma dan perusahaan rantai pendingin mulai memacu distribusi antivirus
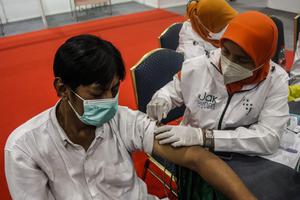
Realisasi vaksinasi Covid-19 saat ini tinggal menunggu waktu. Bahkan Presiden Joko Widodo menyatakan dirinya akan menjadi orang pertama yang diberi vaksin Sinovac pada 13 Januari mendatang.
Namun masih ada potensi pengganjal vaksinasi tersebut, Badan Pengawas Obat dan Makanan (BPOM) belum juga memberikan izin penggunaan darurat (Emergency Use Authorization).
Sementara, Majelis Ulama Indonesia (MUI) telah menyatakan CoronaVac halal dan suci untuk digunakan. Namun, lembaga tersebut belum menetapkan fatwa utuh untuk vaksin Covid-19 tersebut.
Pasalnya, Komisi Fatwa MUI masih menunggu keputusan BPOM terkait keamanan vaksin. Jika vaksin yang digunakan sudah dipastikan keamanannya, maka dua unsur penting dalam penetapan fatwa sudah terpenuhi, yaitu halal dan toyib (aman).
Lalu, sudah sejauh mana kajian BPOM?
Kepala BPOM Penny K. Lukito meyakini EUA vaksin Sinovac bisa diterbitkan dalam waktu dekat. Ia memperkirakan, izin dapat diberikan sebelum 13 Januari sehingga rencana pemerintah untuk vaksinasi pada tanggal tersebut dapat terlaksana.
Penny pun mengatakan, pemerintah memang telah berdiskusi dengan BPOM terkait target dimulainya vaksinasi Covid-19. Namun, dia memastikan hal ini bukan berarti BPOM terikat untuk menerbitkan izin pada tanggal tertentu.
"Sudah ada keyakinan besar sampai hari ini, sehingga masih bisa dipastikan (EUA) akan keluar sebelum 13 Januari," kata Penny dalam konferensi pers di kantornya, Jakarta, Jumat (8/1).
Berdasarkan pedoman Organisasi Kesehatan Dunia (WHO), syarat pemberian EUA ialah vaksin memiliki data uji klinis 1 dan uji klinis 2 setelah enam bulan pengamatan. Selain itu, vaksin harus memiliki data interim uji klinis fase 3 dengan pengamatan selama tiga bulan untuk mengetahui khasiat dan keamanannya.
Khasiat tersebut dapat diketahui berdasarkan data efikasi vaksin. Caranya, mengukur penurunan angka kejadian penyakit pada kelompok orang yang menerima vaksin dibandingkan dengan mereka yang menerima plasebo pada uji klinis fase 3.
Saat ini, aspek keamanan, mutu, dan khasiat telah didapatkan oleh BPOM secara bertahap. Mereka juga telah mendapatkan informasi terkait imunogenisitas vaksin.
Imunogenisitas adalah kemampuan vaksin untuk membentuk antibodi dalam tubuh dan kemampuan untuk menetralisir atau membunuh virus. Dengan data ini, otoritas dapat memprediksi apakah vaksin dapat memberikan perlindungan untuk mencegah penyakit.
Di sisi lain, BPOM masih menunggu data terkait efikasi vaksin Sinovac dari tim uji klinis Universitas Padjajaran, Bandung. Rencananya, hari ini BPOM akan menerima data interim pengamatan tiga bulan uji klinis fase 3. "Hari ini diberikan data paling terakhir yang lengkap dari Bandung," ujar dia.
Setelah itu, BPOM akan segera mengevaluasi aspek efikasi dan membahas hasilnya dengan Komisi Nasional Penilai Obat khusus untuk vaksin Covid-19. Adapun, pembahasan tersebut juga melibatkan pakar, epidemiolog, farmakologi, dokter, dan ahli yang tergabung dalam Indonesian Technical Advisory Group on Immunization (ITAGI).
Penny mengatakan, BPOM berupaya untuk mempercepat proses pemberian EUA. Hal ini dilakukan dengan menyampaikan data industri farmasi dilakukan secara bertahap sejak Oktober 2020.
Hingga Jumat (8/1), pihaknya sudah melakukan rapat evaluasi secara intensif terhadap data yang diperoleh. "Dan segera ada pertemuan final sebelum terbitkan EUA," ujar dia.
Uji Klinis di Bandung
Sebelumnya sejumlah pakar mengkhawatirkan metodologi dan pengambilan sampel uji klinis yang hanya mencapai 1.620 orang. Padahal negara lain seperti Brasil hingga Turki mampu menguji 7.000 hingga 13 ribu sampel.
Namun Penny tak khawatir. Ia menilai, uji klinis vaksin Sinovac di Bandung memiliki desain yang sama dengan uji klinis vaksin yang sama di Brasil dan Turki. Kesamaan tersebut tercermin dari subjek penerima vaksin pada usia 18-59 tahun.
Sejauh ini, uji klinis vaksin Sinovac di Brasil menunjukkan tingkat efikasi sebesar 78%, sementara uji klinis di Turki sebesar 91%. Meski ada selisih yang jauh, Penny tak begitu mengkhawatirkan perbedaan efikasi tersebut.